抗体偶联药物(antibody-drug conjugate,ADC)由靶向特异性抗原的单克隆抗体(antibody)和小分子细胞毒性药物(drug/payload)通过连接子(linker)偶联而成,由于兼具传统小分子化疗的强大杀伤效应及抗体药物的肿瘤靶向性,常被称为“生物导弹”,近年来已成为国内外抗体药物研发新热门方向。
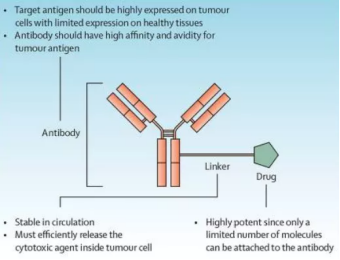
图|From Anish Thomas et al. 2016
根据公开资料,截止目前,全球披露的ADC项目达到339个,中国公司的项目有104个,占比30%。2021年8月8日,荣昌生物与全球ADC药物龙头西雅图基因(Seagen)达成一项26亿美元全球独家许可协议,开发和商业化其抗体偶联药物(ADC)维迪西妥单抗。荣昌生物在此次交易中获得的潜在收入总额将高达26亿美元,刷新了中国制药企业单品种海外授权交易的最高纪录,再次引起了业内外对大热的ADC药物赛道的关注。
ADC药物发展史
早在20世纪初,Paul Ehrlich就首次提出了ADC的概念,并将其描述为“魔法子弹”。然而ADC的发展并非一帆风顺,直到20世纪50年代初才取得重大进展。1958年Mathe首次将抗鼠白细胞免疫球蛋白与甲氨蝶呤偶联用于白血病的治疗,拉开了抗体偶联药物的研究序幕。初步的探索成功却是难以从实验室转化到临床,由于缺乏人源化抗体,再加上提纯制备的难题导致几十年的研究里,没有一个抗体偶联药物的疗效和安全性达到足够要求成为治疗性的药物。
直到 1975年单克隆抗体技术横空出世,第一个现代版的ADC才被报道。十年后抗体人源化技术的诞生,一举解决了抗体制备以及纯化问题。在20世纪80年代到90年代初的时间段ADCs研究也面临一些挑战。
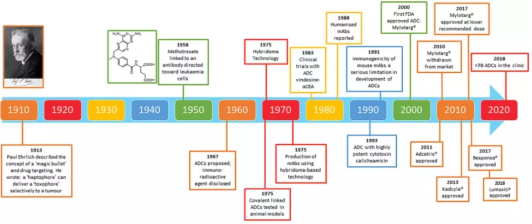
归结其原因有三点,第一:较差的靶标抗原选择性,导致治疗效果较差;第二:嵌合抗体或小鼠抗体的使用,这些抗体可引起免疫原性;第三:较低的细胞毒性分子的有效载荷。在抗体技术进步的同时,偶联策略也在不断发生变化,尤其是对胞吞以及溶酶体的理解,直至2000年美国FDA批准Mylotarg上市。至今已有13个ADC药物被批准上市,Nature预测2026年已上市ADC药物全球市场规模将超164亿美元。
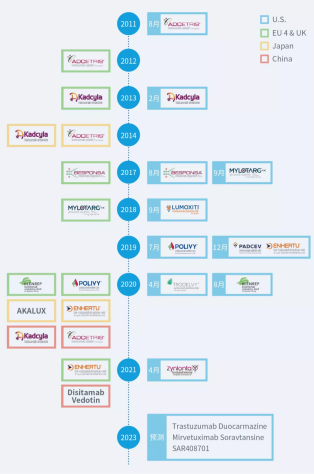
图|ADC在美国EU4&UK、日本、中国获批上市表(数据来源:IQVIA分析)
ADC药物的体内过程和作用机理
一、体内过程
1.识别:ADC药物通过血液循环进入肿瘤组织后,与肿瘤细胞表面的抗原结合。
2. 内化:随后在受体介导下,大多通过网格蛋白的牵引发生内吞,形成核内体。
3. 释放细胞毒分子:氢离子流入核内体形成酸性环境,随后核内体和溶酶体融合,ADC药物被降解,释放细胞毒分子至细胞质中。
4. 细胞凋亡:细胞毒分子与DNA、微管蛋白等结合后,影响其复制或有丝分裂,导致细胞凋亡。
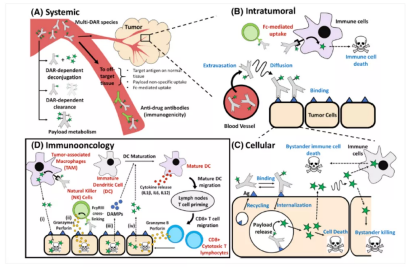
图|From BioDrugs, 2018
二、旁观者(By-stander)效应
ADC药物在癌细胞内释放的药物(或链接子-药物组合物)是可渗透或跨膜,这些释放的药物能够杀死相邻癌细胞,这种现象称为“旁观者效应”。
实体肿瘤细胞抗原的表达通常是异质性,因此,抗体偶联药物可能无法直接有效地杀伤邻近的抗原阴性癌细胞,当抗体偶联药物在癌细胞外或靶细胞内释放细胞毒素后,释放出的小分子药物不仅可以杀死抗原阳性癌细胞,还可以通过旁观者效应杀死附近的其他癌细胞。同时该类药物旁观者效应还破坏了肿瘤生长的环境,如肿瘤基质细胞和肿瘤血管,从而进一步增强杀伤癌细胞作用。
三、高渗透长滞留(EPR)效应
高渗透长滞留效应:指一些特定大小(10~200 nm)的大分子物质(如脂质体、纳米粒以及一些大分子药物)更容易从肿瘤部位血管渗透进入肿瘤组织并长期滞留(和正常组织相比)的现象。
造成EPR效应原因如下:
1.肿瘤部位血管在结构、形态上与正常血管不同,其内皮细胞间隙大,缺少血管壁平滑肌层等;
2.肿瘤血管渗透性因子(如VEGF、缓激肽等 )的释放提高血管通透性;
3.肿瘤组织缺少淋巴管致使淋巴液回流受阻,造成了大分子物质可以方便地穿过血管壁在肿瘤组织中富集,且不被淋巴液回流带走而能长期存于肿瘤组织。
ADC药物开发要素
一、肿瘤靶抗原
肿瘤靶抗原的选择需要考虑以下几个因素:
1.特异性高表达:在肿瘤细胞表面特有或肿瘤细胞相关,高表达,正常组织不表达或少表达;
2.可介导内吞:ADC与抗原结合后可被内吞至细胞内(目前也有一些ADC药物可不经过内吞就能发挥杀伤作用);
3.胞外域:胞外结构域(ECD)尽量少分泌或脱落进入血液循环,以免过早地与ADC结合,中和药效,甚至产生毒副作用。
二、小分子药物(payload)
1.小分子药物决定ADC药效发挥和毒性产生,不仅要求细胞毒性高(pM~nM),同时还要具有良好的化学和物理稳定性以及良好的水溶性;
2.常用的细胞毒性药物效应分子为:
①微管抑制剂:奥利司他汀类(auristatins,MMAE、MMAF、AF)、美登素类(maytansinoids,DM1、DM4)、微管溶素(Tubulysins);
②DNA损伤剂:卡奇霉素(calicheamicin)、多米卡星(duocarmycins)、吡咯并苯二氮䓬类(pyrrolobenzodiazepine,PBDs);
③DNA转录抑制剂:瓢蕈毒素(Amatoxin)和异喹啉生物碱(Quinoline alkaloid,SN-38)。
三、连接子(linker)
1.连接子决定了抗体的连接位点、DAR、偶联药物分布和连接的稳定性;
2.连接方式分为:化学偶联和定点偶联;
化学偶联:容易导致ADC异质性较高。
①利用氨基酸残基侧链(赖氨酸的ε氨基,如Besponsa、Mylotary、Kadcyla);
②先在赖氨酸残基上引入马来酰亚胺;
③还原部分二硫键释放半胱氨酸残基等。
定点偶联:产生更多同质性ADC,质量易于控制。
①可控位点引入半胱氨酸;
②将基因编码氨基酸标签引入抗体;
③用生物正交反应引入非天然氨基酸等。
3.根据细胞内是否被裂解分为可断裂型和不可断裂型,后者血中稳定性更强, 半衰期更长;
可断裂型:
酸敏感型:利用溶酶体和核内体酸性环境水解;
酶敏感型:利用溶酶体中的酶裂解连接子;
谷胱甘肽敏感型:谷胱甘肽还原连接子中的二硫键;
不可断裂型:mAbs在溶酶体内发生降解,释放出带有连接子(如硫醚、马来酰亚胺基己酸)的小分子毒素。
四、抗体和抗体药物偶联比(drug-to-antibody,DAR)
抗体的选择:
①抗体要与靶点亲和力较高(0.1~1 nM),在血中稳定性好,免疫原性和交叉反应性低;
②抗体与抗原结合后可被内吞至细胞内(也可不内吞发挥杀伤作用);
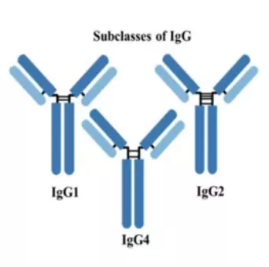
③均为IgG,IgG1(ADCC、CDC)、IgG2和IgG4;
④作为ADC药物的导航系统,抗体本身的药效作用并不十分重要;
⑤整体上抗体选择及开发策略与单纯的抗体药物没有太大差别。
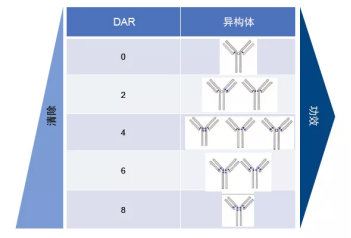
DAR值:
采用化学偶联:因每个抗体具有多个Lys/Cys位点,所以得到含有不同DAR值(0-8)的混合物。体外药效随着DAR的增加而增加,但体内药效不随DAR的增加而增加,可能由于疏水性小分子药物和/或linker增加到一定程度后,ADC疏水作用和清除率增加,毒性越来越高,TI降低。
采用定点偶联:可有效控制DAR值,ADC稳定性更好,聚集性更低。
ADC药物的体内过程特性与研究考量
一、ADME特性
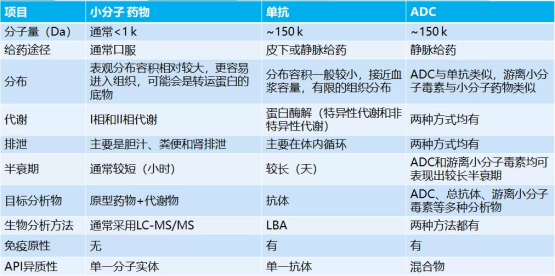
二、DMPK研究的关键考量
1.生物分析方法开发
2.基于小分子drug释放和代谢研究
①释放酶体系的选择,微粒体、肝脏S9、CYP450、et al.
②从ADC解离释放小分子drug的形式,是否携带linker、氨基酸等
③全新小分子drug静脉给药途径的代谢(代谢产物、代谢路径)、排泄等研究
④DDI:代谢酶抑制剂、诱导剂
3.基于ADC药物处置机制的ADME研究
①ADC体循环稳定性(plasma)
②Linker,DAR对ADME特性影响
Ø 理化特性(电荷、亲/疏水)、药效、安全性、PK
③非临床PK研究动物种属
Ø 相关动物选择(基于抗体部分)
Ø 剂量选择以及生物分析对象
④组织分布
Ø 靶组织与非靶组织
⑤代谢及排泄研究
Ø 基于放射标记技术的研究
777永利总区医药针对ADC药物研发的技术服务平台
一、研究条件与经验
777永利总区医药ADC药物研究平台具有支持ADC药物研发立项、工艺和化合物筛选、IND申报不同阶段成熟研究策略和全套解决方案,覆盖药代动力学、药效学、毒理学,同时配备高水平的专业科研团队和一流的技术平台:如LC-MS/MS、LC-QTOF-MS、放射性同位素示踪分析仪、MSD、酶标仪、流式细胞仪等,已与多家大型ADC生物制药企业开展合作,现有多个品种在研,研发和注册经验丰富。
提供MMAE、MMAF、AF、SN-38等常见payload体内分析、体外稳定性、代谢物谱研究的成熟方法和数据
提供曲妥珠单抗、贝伐珠单抗、度伐利尤单抗等针对不同靶点ADC药物的体内分析方法和数据
现有抗HER2单抗+MMAF、抗PD-L1单抗+MMAE等多种ADC药物在研
二、非临床技术服务Package
1. ADC药物立项阶段研究
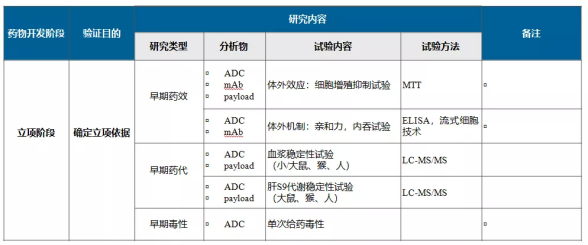
2. ADC药物PCC阶段研究
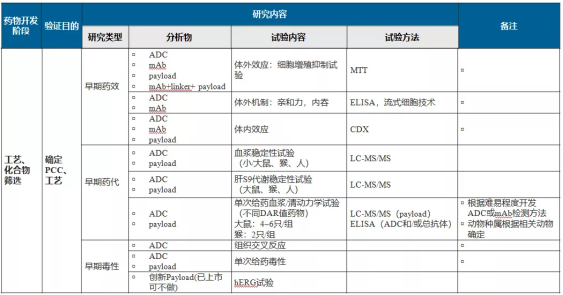
3. ADC药物IND阶段研究内容——药效
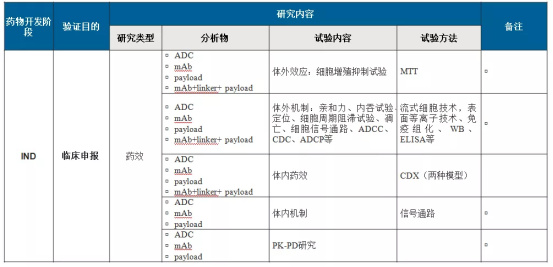
4.ADC药物IND阶段研究内容——药代
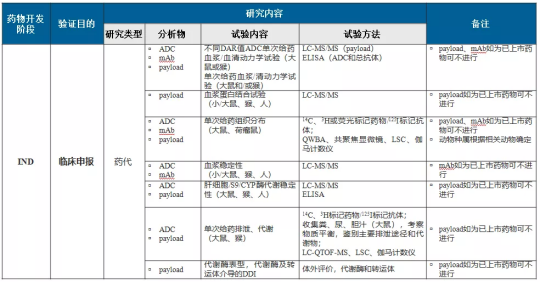
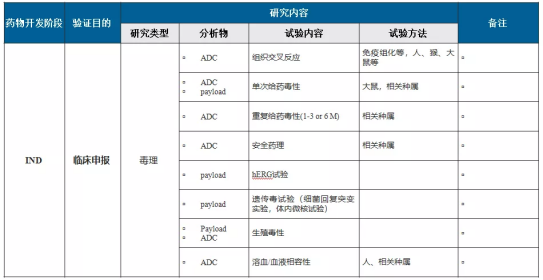
5.ADC药物IND阶段研究内容——毒理